Периодическая система Менделеева – это удивительный инструмент, который был разработан русским химиком Дмитрием Ивановичем Менделеевым в конце XIX века. Она представляет собой упорядоченную таблицу элементов, где они располагаются в порядке возрастания атомных номеров, а их химические свойства повторяются через определённые интервалы – периоды.
Периодический закон в химии, который лежит в основе Периодической системы Менделеева, утверждает, что свойства элементов периодически изменяются с изменением их атомных номеров. Это означает, что элементы схожей группы имеют похожие химические свойства, а элементы одного периода имеют последовательное изменение этих свойств.
Периодическая система Менделеева сыграла огромную роль в понимании химических элементов и развитии химической науки. Она не только позволяет организовать элементы в упорядоченную систему, но и предсказывать их химические свойства, что имеет огромное значение для практического применения.
Благодаря Периодической системе Менделеева мы можем легко определить, какие элементы обладают похожими свойствами и как они взаимодействуют друг с другом в химических реакциях. Это позволяет совершенствовать синтез химических соединений, разрабатывать новые материалы и прогнозировать нужные свойства веществ.
История развития Периодической системы Менделеева
В древние времена существовали различные представления о химических элементах. Однако научная систематизация началась с работы английского химика Джон Долтона в конце XVIII века. Долтон предложил систему классификации элементов на основе их атомной массы.
Следующий важный вклад в развитие периодической системы внес русский химик Александр Бегейсер. В 1863 году он разработал трёхмерную таблицу элементов, где элементы располагались по порядку возрастания атомной массы.
Однако наибольшую известность получил российский химик Дмитрий Менделеев. В 1869 году он представил свою версию периодической системы на основе классификации элементов по их атомным массам и химическим свойствам. Менделеев не только систематизировал существующие элементы, но и предсказал существование новых элементов с определенными свойствами.
Постепенно периодическая система Менделеева была доработана и расширена. С появлением квантовой теории в начале XX века, химики стали понимать, что основной фактор, определяющий свойства элементов, — это количество электронов в их внешних энергетических оболочках. В результате была введена новая система расположения элементов — по их атомным номерам, которые соответствуют количеству протонов в атомном ядре.
В настоящее время Периодическая система Менделеева является одним из самых важных и фундаментальных понятий в химии, которое позволяет химикам понять и предсказать поведение химических элементов и их соединений.
Первые предпосылки к созданию системы элементов
Уже в древности химики замечали, что некоторые элементы обладают схожими свойствами и могут группироваться в определенные классы. Например, Греки заметили, что металлы могут быть источниками света и тепла, тогда как неметаллы не обладают такими свойствами.
Следующий важный шаг в направлении создания системы элементов сделал английский химик Джозеф Пр
Открытие Менделеевым периодического закона
Периодический закон в химии был открыт русским химиком Дмитрием Ивановичем Менделеевым в 1869 году. Он разработал систему классификации химических элементов, которая получила название «Периодическая система Менделеева». Эта система основана на периодическом возрастании атомных масс элементов и позволяет представить их в виде таблицы.
Главным открытием Менделеева стало то, что он смог предсказать существование ещё неизвестных элементов и даже указать их основные свойства. Для этого он оставлял пустые места в таблице, которые со временем были заполнены открытыми новыми элементами.
Периодический закон утверждает, что свойства химических элементов изменяются периодически с возрастанием атомной массы. Это означает, что элементы с похожими химическими свойствами периодически повторяются через определённые промежутки. Это позволяет упорядочить и систематизировать знания о химических элементах и предсказывать свойства новых элементов.
Открытие Менделеевым периодического закона стало важным прорывом в химии и существенно повлияло на развитие науки. Благодаря этому открытию химики получили новые инструменты для изучения и понимания мироздания на атомарном уровне.
Современное состояние и применение Периодической системы
Современная Периодическая система включает в себя 118 элементов, упорядоченных по возрастанию атомного номера, который определяется числом протонов в атоме элемента. Каждый элемент имеет свой уникальный химический символ, например, водород (H), кислород (O), железо (Fe) и так далее.
Периодическая система помогает химикам не только классифицировать элементы, но и предсказывать их химические свойства и поведение. Она позволяет строить графическую модель элементов, основанную на их электронной конфигурации, что позволяет предсказывать и анализировать взаимодействие элементов при химических реакциях и образовании соединений.
Периодическая система также играет важную роль в обучении химии и научных исследованиях. Она используется для описания и объяснения реакций и свойств элементов, разработки новых материалов, прогнозирования поведения элементов в различных условиях и многое другое. Кроме того, она оказывает влияние на различные области науки и технологии, такие как медицина, материаловедение, энергетика, электроника и окружающая среда.
Структура Периодической системы Менделеева
Периодическая система Менделеева представляет собой организацию химических элементов в виде таблицы, которая отражает закономерности в их свойствах и структуре. Структура этой таблицы основана на атомных номерах элементов и демонстрирует повторение закономерностей через периоды (горизонтальные строки) и группы (вертикальные столбцы).
Периоды в Периодической системе представляют атомные оболочки элементов и указывают на количество электронов, находящихся на этих оболочках. В первом периоде находятся элементы с одной электронной оболочкой, во втором периоде – с двумя, и так далее. Каждый последующий период начинается с элемента, у которого заполняется следующая электронная оболочка.
Группы в Периодической системе организуют элементы сходными химическими свойствами в вертикальные столбцы. Они обозначаются числами от 1 до 18 или буквами от A до H и представляют различные категории элементов. Некоторые из групп имеют особое название, например, группа 1 (Iуп. B) содержит щелочные металлы, а группа 17 (VII ап. H) – галогены.
Структура Периодической системы Менделеева также отображается с помощью блоков, которые указывают на характерные свойства элементов. В частности, внешний блок Периодической системы представляет блок п, блок p, блок f и блок d. Блок s находится слева от Периодической системы и следует за блоком f.
Таким образом, структура Периодической системы Менделеева предоставляет визуальное представление периодического закона и отражает взаимосвязь и закономерности между химическими элементами, что полезно для изучения химии и понимания их реактивности и свойств.
Периоды и группы
Периодическая система Менделеева представляет собой удобный способ организации химических элементов. Элементы в периодической системе располагаются в порядке возрастания атомного номера, а также в соответствии с их сходством в химических свойствах.
Периоды — это строки элементов в периодической таблице. Количество элементов в каждом периоде соответствует количеству электронных уровней у атома. Например, первый период содержит только два элемента — водород и гелий, поскольку они имеют один электронный уровень.
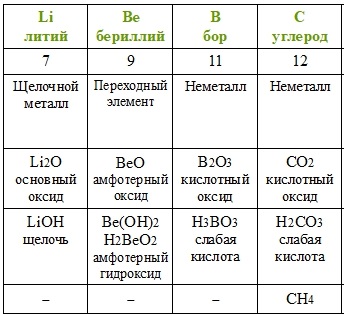
Группы — это столбцы элементов в таблице. Группы объединяют элементы с похожими химическими свойствами. Например, элементы группы 1, такие как литий, натрий и калий, являются щелочными металлами и имеют сходные свойства.
Периодическая система Менделеева также отражает периодический закон, согласно которому химические и физические свойства элементов изменяются периодически с увеличением атомного номера. Это связано с изменением строения атомов и их электронной структуры.
Каждый элемент периодической системы Менделеева имеет свой номер, атомный номер, символ и атомную массу, которые указываются в соответствующих ячейках таблицы. Также элементы могут иметь дополнительные химические и физические свойства, которые могут быть указаны в отдельных ячейках.
| Период | 1 | 2 | 3 | 4 | 5 | 6 | 7 | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Группа 1 | H | Блок d | ||||||||||
| Группа 2 | He | Блок f | ||||||||||
| Группа 3 | Li | Блок p | ||||||||||
| Группа 4 | Be | Блок s | ||||||||||
| Группа 5 | B | Блок f | ||||||||||
| Группа 6 | C | Блок d | ||||||||||
Атомная масса и атомный номер
Атомная масса выражает массу атома в атомных единицах и зависит от числа протонов и нейтронов в ядре, а также от количества электронов на энергетических уровнях. Обычно атомная масса указана в элементной клетке периодической таблицы и представляет среднее значение массы атомов данного элемента, учитывая обилие его изотопов.
Атомная масса и атомный номер организованы в периодическую таблицу таким образом, что они возрастают с левого верхнего угла до правого нижнего угла. Это способствует систематизации и классификации элементов по их физическим и химическим свойствам. Зная атомный номер и атомную массу элемента, можно предсказать его химическое поведение и реакционную способность.
На основе атомной массы и атомного номера, периодическая система Менделеева позволяет систематизировать и классифицировать элементы, определять их свойства и устанавливать закономерности в их химическом поведении. Эти два свойства являются основными характеристиками элементов и играют важную роль в изучении и понимании химии.
Химические свойства элементов
Химические свойства элементов определяются их электронной конфигурацией и количеством электронов во внешнем энергетическом уровне.
Внешний энергетический уровень, также известный как валентный уровень, играет важную роль во взаимодействии элементов с другими веществами. Количество электронов на валентном уровне определяет химическую активность элемента и его способность образовывать химические связи с другими элементами.
Клавишевые элементы, находящиеся в левой части Периодической таблицы, обладают малым количеством валентных электронов и обычно образуют положительные ионы. Эти элементы хорошо взаимодействуют с элементами с большим количеством валентных электронов, такими как кислород, сера или хлор.
Валентные электроны можно представить как ключи, которые могут открыть или закрыть входные двери в другие элементы. Когда валентные электроны образуют соединение с другим элементом, они образуют химическую связь. Это может быть ионная, ковалентная или металлическая химическая связь.
Вопрос-ответ:
Что такое периодическая система Менделеева?
Периодическая система Менделеева — это таблица, которая систематизирует химические элементы по их атомным номерам, электронной конфигурации и химическим свойствам.
Как строится периодическая система Менделеева?
Периодическая система Менделеева строится по принципу расположения элементов в порядке возрастания атомных номеров. Вертикальные столбцы называются группами, а горизонтальные строки — периодами. Элементы в одной группе имеют схожие химические свойства.
Кто создал периодическую систему Менделеева?
Периодическую систему Менделеева создал русский химик Дмитрий Иванович Менделеев в 1869 году. Он систематизировал известные на тот момент химические элементы и предсказал существование тогда еще не открытых элементов.
Какие данные включает периодическая система Менделеева для каждого элемента?
Периодическая система Менделеева для каждого элемента включает его атомный номер, символ, относительную атомную массу, электронную конфигурацию и химические свойства.
Зачем нужен периодический закон в химии?
Периодический закон в химии нужен для систематизации и упорядочивания информации о химических элементах. Он позволяет предсказывать свойства неизвестных элементов и находить закономерности в химических реакциях. Также он является основой для изучения и понимания различных химических процессов и важен для развития химической промышленности.
Что такое периодическая система Менделеева?
Периодическая система Менделеева — это упорядоченная таблица химических элементов, в которой эти элементы располагаются по возрастанию атомных номеров и структуре их атома. Эта система позволяет классифицировать и организовать все известные химические элементы в соответствии с их химическим и физическим свойствами.
Какие элементы включает периодическая система Менделеева?
Периодическая система Менделеева включает все известные химические элементы — от самых простых, таких как водород и гелий, до самых тяжелых, таких как унунпентий и унунтрий. Всего в периодической системе содержится 118 элементов.
